“合规”不是终点:构建中国药企出海的差异化资产
中国生物制药行业正处于一个前所未有的历史机遇期。2025年对外授权交易(License-out)全年总金额突破1350亿美元,超过了过去三年的总和,创下历史新高。与此同时,中国本土药企也在加速从单纯的Biotech向Biopharma,乃至全球性跨国药企(MNC)跨越。
然而,生物制药的复杂性和高风险特征,使得中国药企在出海过程中不仅要面对更加严苛的监管要求,还要在精细化操作和科学化决策上下苦功。质量管理已不再仅仅是企业的合规底线,更是中国药企通往全球市场的“通行证”,以及构建差异化竞争优势的核心资产。
日前,Veeva中国质量战略负责人卢文洁女士聚焦“中国药企质量数智化走向国际:构建面向未来的GMP管理新范式”分享了Veeva观点,并介绍了Veeva质量云产品的赋能价值。
直面创新药质量管理的“孤岛”痛点
尽管中国药企在研发创新上突飞猛进,但在质量管理的数智化基建上,仍面临着许多痛点。如果不能有效应对,将在出海过程中转化为巨大的合规成本与信任危机。
01 数据孤岛与流程“黑盒”
在传统模式下,研发、临床、生产制造、质量、注册及药物警戒等系统彼此割裂,无法实时共享与验证数据。同时,还有不少企业仍在大量使用Excel、纸质文档或邮件,管理复杂的质量流程。这导致质量风险无法快速溯源,注册申报资料整理效率极低,数据完整性面临审计风险,更难以生成高效与直观的决策洞察。
02 依赖人工经验,预警“失灵”
许多企业的质量检测仍停留在“事后检验”阶段,偏差或OOS/OOT发生后才开始调查,不仅处理周期长,也导致了巨大的生产损失。由于缺乏基于大数据的分析工具,质量决策高度依赖个人的“老师傅经验”,而非客观的数据证据。这种被动响应模式无法实现风险的预警和拦截。
03 国际化合规挑战
创新药出海需满足FDA、EMA等全球最严格的cGMP标准,对全生命周期数据的可追溯性和可靠性要求极高。然而,中国药企普遍缺乏能够满足多国法规要求的统一质量管理体系,导致国际化进程受阻,高昂的合规成本和不确定性成为制约。特别是在数据完整性(ALCOA+)和质量管理体系的动态有效性方面,中国药企与国际标准仍有差距,难以获得海外监管机构的信任。
构建端到端的质量云生态
针对传统体系中实时、可信数据缺失的瓶颈,Veeva认为药企亟需向“质量4.0”范式转型——以ICH Q10确立的药品质量体系模型为基准,通过对数字化技术、业务流程和人员的数智化重塑,构建一个以云架构、大数据和互联互通为特点的数智化质量管理体系。
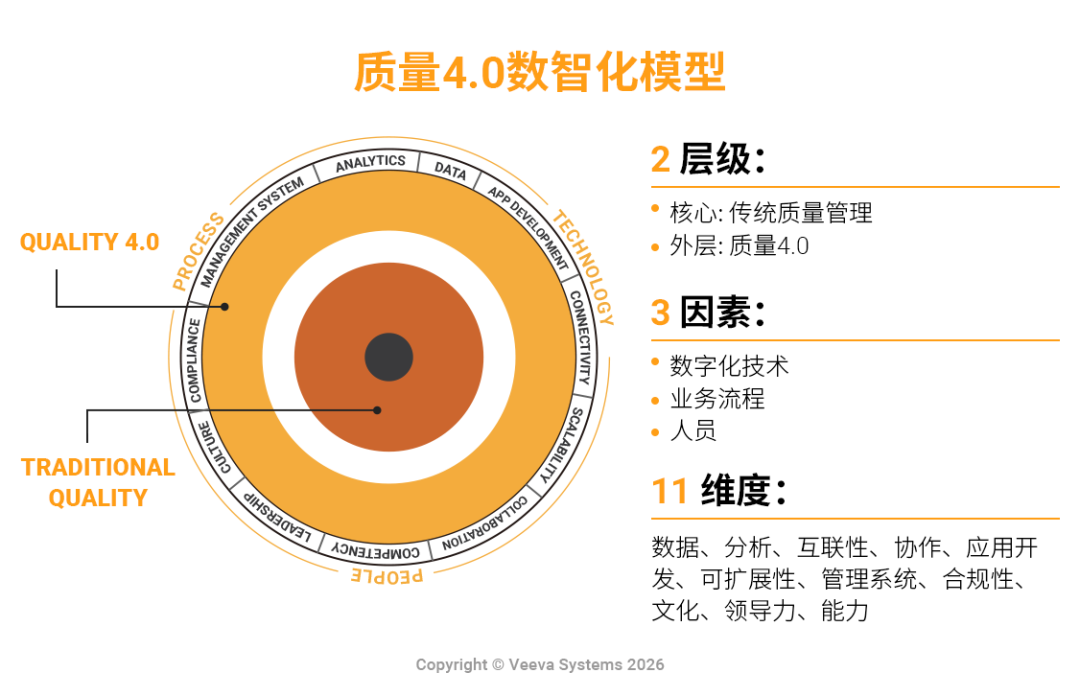
这并非简单的工具升级,而是将质量管理从“合规成本”转向“差异化资产”。基于这一模式,Veeva打造了一个包含QA、QC、培训、验证管理、实验室管理及批次释放等在内的“大质量”生态,帮助药企实现从“文档管理”到“数据驱动”、从“流程隔离”到“端到端贯通”、从“被动响应”到“主动预测”的转变。
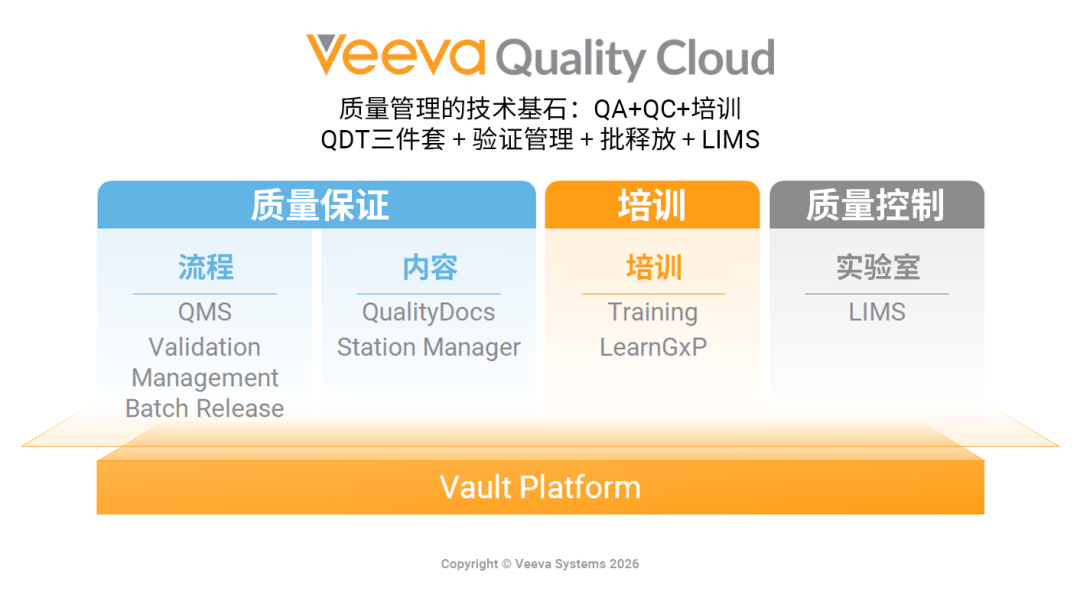
原生联动:Veeva QDT的一体化价值
QDT(流程、文档、培训)是质量体系的核心支柱。不同于传统模式下多供应商系统拼接导致的接口延迟与证据链断裂,Veeva实现了“一个平台、一个数据源”的原生整合。在这种生态下,管理不再是孤立动作:一旦触发变更控制,系统会自动关联并提醒受控SOP的修订,并同步指派全员再培训任务。这种“牵一发而动全身”的自动化闭环,有效避免了跨系统转录的人为差错,确保了单一事实来源(SSOT)的权威性。
重塑验证范式:从文档驱动到数据驱动
传统的验证往往是文档驱动的,这导致纸质报告堆积如山。而“验证4.0”强调以数据为中心,实现持续的确认和验证。无论是计算机系统验证、设备验证、工艺验证,清洁验证还是实验室方法验证,系统都能根据预设的频次自动提醒回顾,确保验证状态的持续受控。

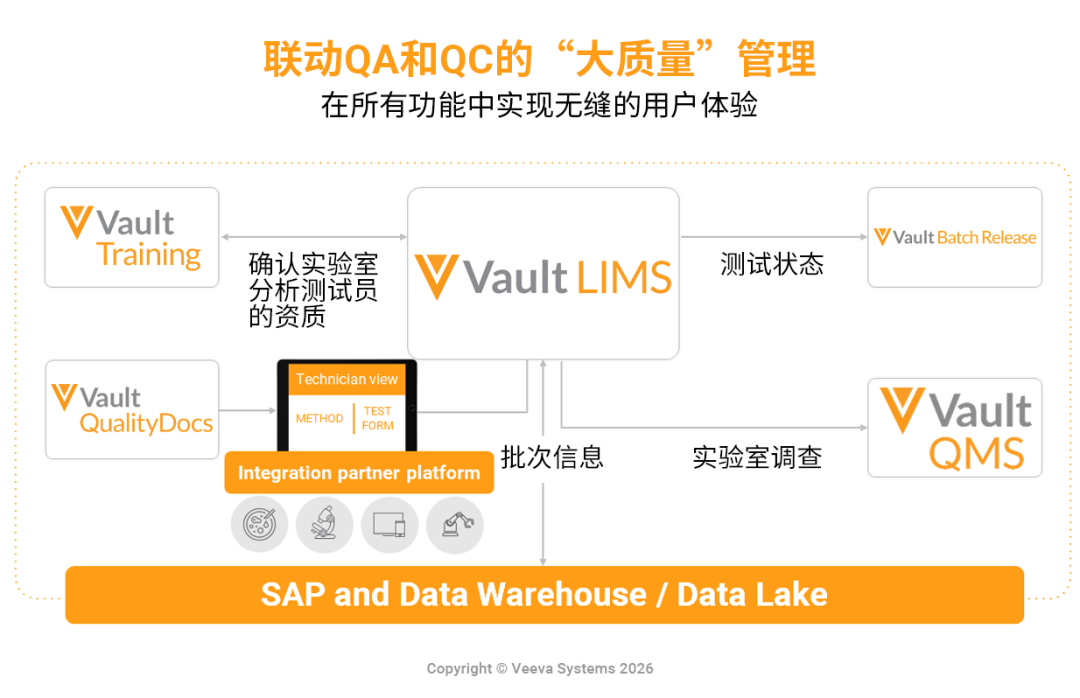
打通实验室断点:QA与QC的深度融合
实验室是质量数据的核心产地,但传统的质量保证(QA)与质量控制(QC)系统和流程脱节,导致检测执行透明度不足,技术成本与复杂性也居高不下。Veeva的LIMS解决方案涵盖了样品管理、测试执行、稳定性考察等QC核心功能,更可以与QA端的QMS、QualityDocs、Training等系统无缝集成,真正做到全覆盖、一体化。这意味着当实验室发生OOS(超标)时,系统可以自动在QMS中发起偏差流程,无需跨系统搬运数据,实现了QC与QA的协同作战。
决策枢纽:智能化的批次释放
批次释放(Batch Release)是连接生产与上市的关键环节。它像一个集成“驾驶舱”,汇集了批记录、变更、偏差及实验室数据等所有关键信息。每一批药都能“自动讲述自己的故事”。质量受权人(QP)不再需要翻阅如山纸堆,而是基于准确的结构化数据做出快速放行决策,加速创新药在全球市场的上市进程。

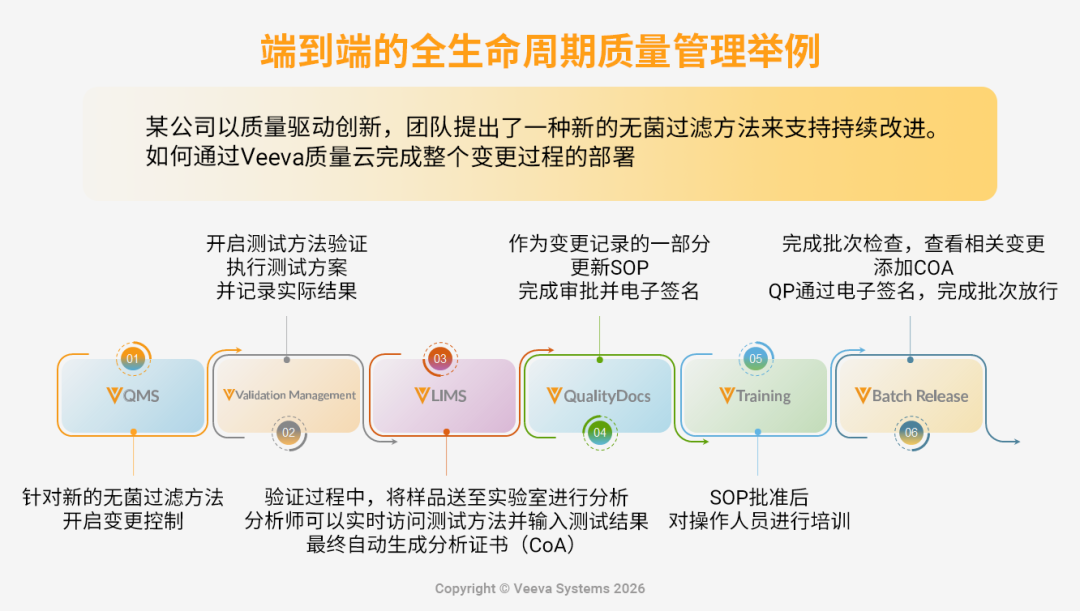
场景Demo:端到端全生命周期质量管理
基于团队提出的“无菌过滤方法”,某生物制药公司依托Veeva“大质量”平台实现了端到端的数智化联动。从变更控制的开启到受控SOP的自动修订,再到指派全球再培训,全过程闭环透明。这不仅确保了全球质量标准的统一,更显著提升了全球范围内的变更执行效率,让先进工艺得以安全、合规地加速落地。
“质量人”在数智化时代的四重角色
数智化转型不仅是技术升级,更是人才专业素养的重塑。style=”color:var(–colormain)”“质量人”需要实现从传统“质量保证(QA)”到“质量智慧(QI)”的转型——他们不再是按下“暂停键”的“监察”,而是能够按下“加速键”的、更具战略价值的新角色。
1 业务与技术的“翻译官”
质量人员需在业务需求与技术实现之间架起桥梁,将晦涩的法规要求转化为IT系统可执行的功能逻辑,并在合规前提下推动流程的简化与优化。
2 数据资产的“守护者”
高质量的数据是算法与决策的基石。面对海量数据,质量人员的核心职责转变为捍卫数据的单一事实来源与数据完整性,赢得监管机构与合作伙伴的信任。
3 数智文化的“倡导者”
数智化不仅是技术的引入,更是文化的变革。质量管理者需在组织内部倡导数智化文化,推动合规意识内化为员工的无意识行为,利用系统工具降低人为风险。
4 动态风险的“领航员”
这是最高阶的要求。基于结构化的大数据,质量人员应具备更敏锐的风险洞察力,利用趋势分析与数据模型,主动识别并拦截潜在风险,为企业的全球化保驾护航。
在全球生物制药竞争格局重塑的当下,质量数智化已不再是锦上添花的“可选项”,而是中国药企出海的“必选项”。通过构建端到端的质量云平台,打通研发、生产到上市的全链路数据,中国药企不仅能够从容应对国际监管机构的严格审计,更能通过降本增效提升全球竞争力,在未来十年的出海博弈中掌握主动权。

