大部分合同研究组织表示eTMF技术能够加速研究的启动步伐,这正是促使他们使用该技术的主要原因
马萨诸塞州波士顿-2015年9月16日 — 今天,《2015年Veeva无纸化TMF调查:年度合同研究组织报告》在第七届临床试验外包新英格兰地区会议上发布,报告显示与一年前相比,使用电子试验主档案(eTMF)应用的合同研究组织数量显著攀升。这项对全球TMF持有机构的研究发现,受访的合同研究组织中有38%正在使用eTMF应用,而2014年仅有21%。eTMF应用带来的诸多益处促使合同研究组织采用该技术。一半以上(58%)的受访者表示采用eTMF技术的主要原因是此技术能够加快研究的启动,50%的受访者称eTMF技术有助于节约成本。The
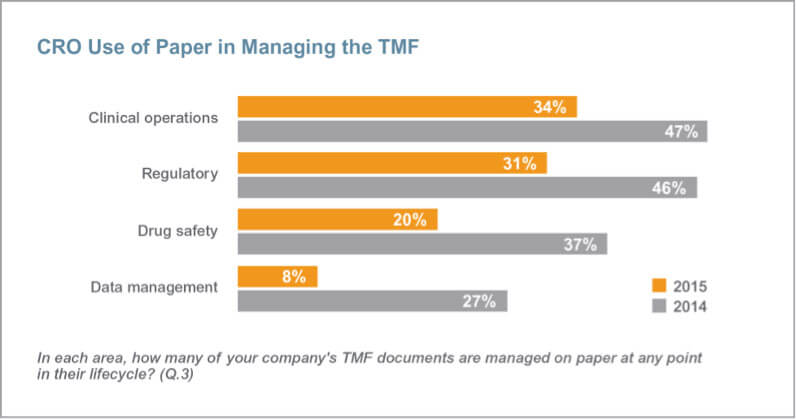
这项针对全行业的研究还显示大量合同研究组织正在抛弃有纸化流程。受访的合同研究组织正在如临床运营、合规、药品安全和数据管理等涉及大量内容的领域使用电子化流程。数据管理领域的变化明显,有纸化流程的使用率从2014年的27%下降到2015年8%。临床运营领域集中了数量多的TMF文档,其有纸化流程的使用率从2014年的47%锐减至2015年的34%。
采用eTMF解决方案的合同研究组织报告称该技术带来了一系列益处,涉及TMF的方方面面。例如,大部分合同研究组织的检查准备情况都有所改善,减少了缺失文档(92%)、归档错误(89%)、重复文档(86%)、不完整文档和/或签名缺失(84%)以及过期文档(81%)的数量。此外,超过一半(57%)的受访者报告称eTMF改善了其在应对审计和检查方面的准备情况。
Advanced Clinical负责临床运营的执行副总裁Julie Ross表示:“过去两年多以来,eTMF应用以前所未有的速度,在生命科学行业流行起来。很少有人要求 Advanced Clinical提供除eTMF服务以外的其他服务,因为eTMF的益处非常明显。客户和合同研究组织可以实时获取结果,完全一目了然,还可以对研究进行控制,这全面提高了审计准备情况。”Advanced Clinical是全球优秀的药品研发服务供应商。
当被问到使用指标以缩短临床试验时间所带来的潜在影响时,大部分合同研究组织都表示,能够了解与研究启动相关的流程为其带来的益处显著。三分之二(70%)以上的合同研究组织认为获取从研究基地部分到机构审查委员会核准所需时间的信息非常重要。68%的合同研究组织表示,获取关于收集必要的现场文件所需时间的信息很重要。
对受访合同研究组织中TMF指标使用情况的研究发现,16%的合同研究组织“经常”使用TMF指标改善试验流程,40%的合同研究组织“有时”使用TMF数据。随着越来越多的组织使用更成熟的eTMF应用,为改善研究流程而使用指标的合同研究组织数量有望上升。《2015年Veeva无纸化TMF调查:年度报告》全文显示采用eTMF应用的合同研究组织与采用使用本地货云端文档系统管理TMF的组织相比,“经常”使用指标的可能性高出了一倍。
“eTMF应用使得现在的临床领导者所获取的大量信息能够得到充分利用。”Veeva的合同研究组织联盟总监Mike Burton表示。“我们有大量的机会改善整个临床流程,但由于没有指标,常常难以发现薄弱之处。然而,先进的eTMF应用却可以快速揭露常见的瓶颈问题和流程效率低下的问题,从而有助于加速研究启动的步伐并最终提高研究质量。”
Burton将在美国东部时间9月16日周三下午3点15分举行的临床试验中的外包新英格兰地区会议第二分会上分享《2015年Veeva无纸化TMF调查:年度合同研究组织报告》的全部结果。与会人员可以前往Veeva展台(#6)领取一份报告,还可以点击 《2015年Veeva 2015 无纸化TMF调查:合同研究组织报告》下载报告。
更多信息:
关于Veeva
Veeva Systems是全球生命科学行业基于云计算模式的商业解决方案领导者提供商,致力于提供创新的技术架构,卓越的产品服务,以及遵循让客户成功的服务理念。目前,Veeva在全球范围内拥有超过275家企业客户,这些客户中有全球大型制药公司,也有新兴的生物技术公司。Veeva总部设在美国旧金山湾区,并在欧洲、亚洲和拉丁美洲设有办事处。更多信息,请访问:www.veeva.com。
前瞻性声明
本新闻稿中载列了前瞻性声明,内容涵盖市场对Veeva产品和服务的需求和认可、使用Veeva的产品和服务所取得的效果,以及一般商业情况,尤其是生命科学行业的商业现状。本新闻稿中载列的任何前瞻性声明都基于Veeva的历史业绩和当前计划、估算业绩和预期而做出,并不代表一定会实现这些计划、估算业绩和预期。本前瞻性声明是Veeva发布本新闻稿之时的预期,可能需要根据后续事态发展做出变更,但Veeva无义务在今后更新本声明。在做出本前瞻性声明之时,存在多种已知和未知的风险及不确定性,有可能造成实际结果与预期相去甚远。在截至2015年7月31日对10-Q 表的备案文件中,“风险因素”和“管理层对财务状况和运营结果的讨论与分析”部分列出了可能影响Veeva财务结果的其他风险和不确定性。该文件载于公司官网:www.veeva.com“投资者”一栏及美国证券交易委员会网站 www.sec.gov。欲了解更多有关可能影响实际业绩的潜在风险,请参阅Veeva向美国证券交易委员会提交的其他备案文件。
联系人:
Lisa Barbadora
公关部:
Veeva Systems Inc.
610-420-3413
pr@veeva.com

