VEEVA RIM
통합 RIM을 통한
허가 혁신
단일 플랫폼에서 포괄적인 허가 정보를 관리합니다.
Veeva RIM
Veeva RIM은 단일 클라우드 기반 플랫폼으로 글로벌 허가 프로세스를 간소화하여 생명과학 기업이 가시성, 데이터 품질 및 민첩성(agility)을 개선할 수 있도록 지원합니다.
시판 속도
변화하는 허가 요건에 신속하게 대응하고 규제기관 문서 제출 계획에서 게시(publish)까지 프로세스 효율성을 높입니다.
컴플라이언스 강화
팀이 높은 데이터 무결성을 갖춘 신뢰할 수 있는 규제 컨텐츠를 개발하도록 확인합니다.
전 세계 업무 조율
단일 RIM 시스템 내에서 HQ, 계열사 및 파트너 전반에 걸친 규제 업무를 조율합니다.
통합 및 연결
Veeva Development Cloud 내에서 다기능 비즈니스 프로세스를 처리합니다.
Veeva Registrations
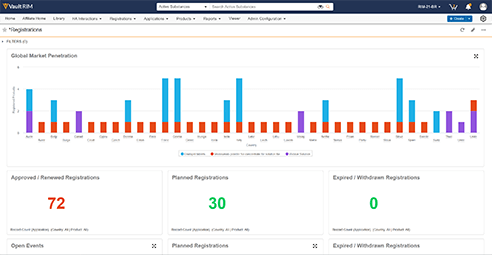
Veeva Registrations는 등록 상태, 변동 사항, 보건 당국 상호 교류 등의 제품 등록 데이터를 전 세계적으로 관리합니다. Veeva의 유연한 데이터 모델은 IDMP 데이터 포인트를 수용하며 변화하는 허가 데이터 표준을 앞으로도 계속 지원합니다. Veeva의 IDMP 접근 방식에 대한 짧은 비디오 시청하기
자세히 알아보기Veeva Submissions
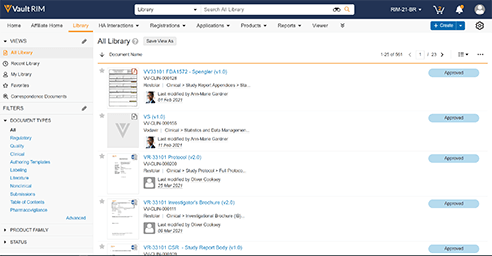
Veeva Submissions는 허가 프로세스를 자동화하여 승인으로부터 규제기관 문서 제출 계획에 이르는 단계를 간소화합니다. 사용자는 제출 컨텐츠 계획을 작성하고, 규제기관 제출에 준비된 문서를 렌더링하며, 완전한 추적성(traceability)을 통해 규제기관 문서 제출 상태를 추적할 수 있습니다.
자세히 알아보기Veeva Submissions Publishing
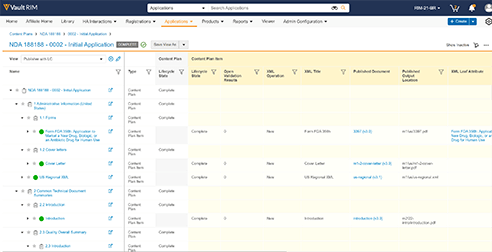
Veeva Submissions Publishing는 포괄적인 규제기관 문서 제출 개발을 위해 Veeva RIM 내에서 게시 기능을 통합합니다. 연속성 있는 퍼블리싱 프로세스를 도입하여 문서를 작성, 밸리데이션 및 제출함으로써 사용자는 규제기관 문서 제출 속도를 크게 높일 수 있습니다.
자세히 알아보기Veeva Submissions Archive
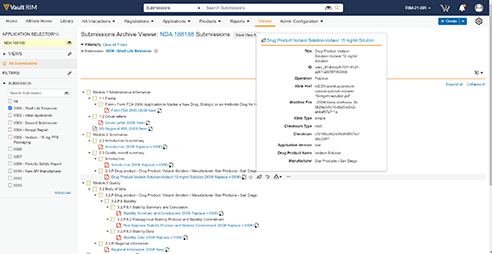
Veeva Submissions Archive는 허가 제출 문서를 클라우드에 안전하게 저장합니다. 소속 관계사는 현지에서 재사용하기 위해 기존 제출 문서 또는 제출 문서 구성 요소를 다운로드할 수 있으며, 이미 보건 당국에 제출되었던 문서들을 업로드할 수 있습니다.
자세히 알아보기Veeva Connections

Veeva Connections는 Veeva에서 제공하는 통합 기능으로, Vault 간에 데이터와 문서를 원활하게 전송합니다. 허가팀의 경우 Veeva RIM to Clinical Operations Connection 를 통해 제품, 연구 및 시험기관 정보를 자동으로 공유할 수 있으며, Vault Quality to RIM Connection를 통해 변경관리 이벤트 생성부터 구현에 이르는 전체 일정을 단축할 수 있습니다. 또한 Veeva RIM to PromoMats Connection은 보건 당국에 직접 게시할 수 있도록 컴플라이언스 패키지 생성을 통합합니다.
이용 가능한 Veeva Connections의 전체 목록을 보려면 Veeva Development Cloud 페이지를 방문하십시오.
Veeva RIM 리소스




