Veeva SafetyDocs
규제 준수 걱정 없는 약물감시 컨텐츠 및 프로세스 관리
SafetyDocs는 약물감시 관련 컨텐츠 및 프로세스를 관리합니다. 이는 약물감시 시스템 마스터 파일(PSMF), 약물감시 협의서(PVA), 위험 관리 계획(RMP) 및 추가 위험 최소화 조치(aRMM), 통합 보고서, 문헌 기사, 그리고 약물감시 징후 조사의 관리를 위한 솔루션을 제공합니다.
Veeva SafetyDocs를 활용하여 어떻게 더 효율적으로 약물감시 컨텐츠 및 프로세스 관리를 수행하는지 자세히 알아보세요.
Announced 2019 Status Mature Customers 11-50
Overview
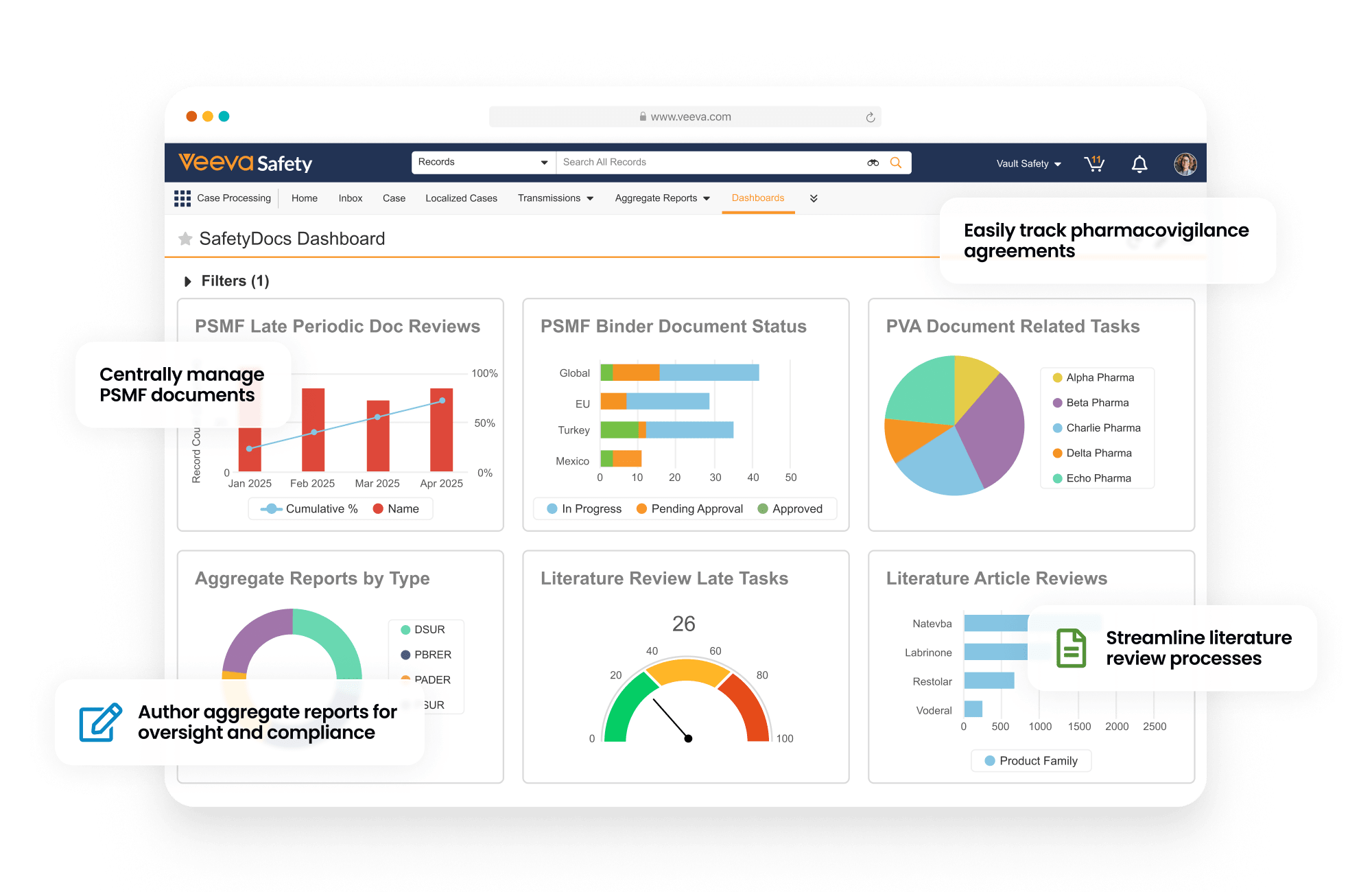
규제 준수 걱정 없는 약물감시 컨텐츠 및 프로세스 관리

SafetyDocs는 약물감시 관련 컨텐츠 및 프로세스를 관리합니다. 이는 약물감시 시스템 마스터 파일(PSMF), 약물감시 협의서(PVA), 위험 관리 계획(RMP) 및 추가 위험 최소화 조치(aRMM), 통합 보고서, 문헌 기사, 그리고 약물감시 징후 조사의 관리를 위한 솔루션을 제공합니다.
Veeva SafetyDocs를 활용하여 어떻게 더 효율적으로 약물감시 컨텐츠 및 프로세스 관리를 수행하는지 자세히 알아보세요.
Veeva SafetyDocs를 선택해야 하는 이유
운영 효율성 및 컴플라이언스 강화
고객 성공 사례
약물감시 전용으로 설계된 검증된 솔루션을 통한
안전 관련 프로세스 및 컨텐츠 관리