Features Brief
Veeva Site Connect Features Brief
간결하고 표준화된 스폰서-시험기관 협업
Veeva Site Connect는 스터디 스타트업, 실행 및 종료 과정에 걸쳐 시험기관과의 정보 흐름을 자동화함으로써 스폰서와 시험기관이 임상시험을 위해 협력할 수 있도록 지원합니다.
이와 같은 정보 흐름에는 프로토콜, 필수 문서 패키지, 안전성 보고서 및 비용 지급 서신이 포함됩니다. 연구 종료 시, 완료된 CRF를 포함한 필수 자료가 전송됩니다. 송수신되는 정보는 eTMF 내에 자동으로 저장됩니다.
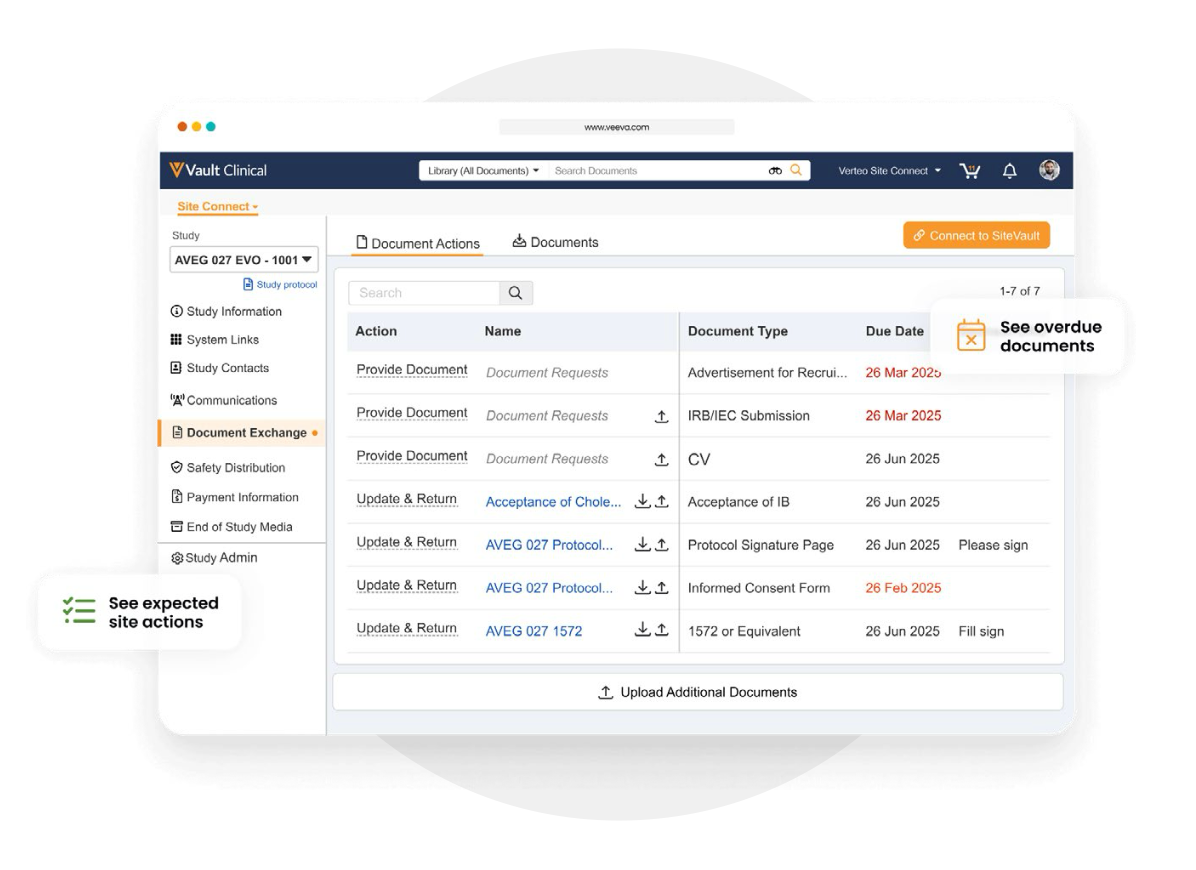
시험기관들은 Site Connect를 통해 업무, 문서, 데이터를 관리합니다. 시험기관들은 선택적으로 SiteVault를 연결하여 향상된 기능을 활용할 수 있습니다.
특장점
- 시험기관과 스폰서의 협업을 위한 하나의 시스템
스폰서는 하나의 애플리케이션에서 임상시험 전체 주기에 걸쳐 모든 기관과 협업할 수 있습니다. 시험기관은 스폰서에 관계없이 동일한 최적화된 사용자 인터페이스에서 작업하며, 모든 임상시험에서 표준화된 작업 방식을 갖게 됩니다.
- 어디서든 모든 기관이 사용 가능
Veeva Site Connect는 전 세계 모든 기관에서 접근 가능합니다. Veeva SiteVault를 eISF로 사용하기로 결정한 시험기관은 원활한 양방향 문서 교환을 위해 연구를 연결하는 추가적인 이점을 얻습니다.
- 더 빠르고 고품질의 임상시험
시험기관-스폰서 협업을 간소화하고 표준화함으로써, 스폰서와 시험기관은 행정적 부담을 줄여 더 낮은 비용으로 고품질의 임상시험을 수행할 수 있습니다.
주요 기능
- 문서 교환
스터디 착수 기간 동안 시험기관 문서를 자동으로 관리하고 배포하여 스터디 스타트업을 가속화합니다.
- 시스템 링크
단일 페이지에서 모든 연구 시스템에 대한 시험기관의 접근을 간소화합니다.
- 안전성 서신 배포
시험기관으로 전송되는 중요한 안전성 서신 정보의 전달 및 추적을 보장하고, 책임 연구자가 정보를 계속 받을 수 있도록 지원합니다.
- 연구 공지
마감일, 주요 날짜 및 알림과 같은 중요한 공지사항을 모든 시험기관에 공유합니다.
- 비용 지급 정보
임상연구 시험기관에 상환 데이터 및 연구비 지급 서신을 전달하고 Veeva Clinical Operations 내에서 시험기관 인보이스를 직접 수신합니다.
- 종료된 임상연구 데이터
완료된 CRF 출력물과 같은 최종 피험자 데이터를 EDC에서 임상연구 시험기관으로 가져오고, 배포하고, 추적합니다. 이는 eTMF에 자동 파일링하는 기능을 포함합니다.
- 연구 정보
연구 이름, 설명, 시험기관 번호, 그리고 프로토콜 링크와 같은 연구 정보를 한 곳에서 편리하게 열람합니다.
- eTMF 및 eISF 연결성
시험기관은 선택적으로 Veeva SiteVault를 사용하여 임상 문서가 Veeva Clinical Operations와 자동으로 교환되도록 할 수 있습니다. 이는 스폰서 TMF 및 시험기관 ISF 조정 활동과 관련된 수동 단계를 줄입니다.
- 연구 연락처 및 시험기관 주소
시험기관에 역할, 이름, 전화번호, 이메일 등 자신의 연구와 관련된 연락처 정보를 제공하고, 주소를 포함한 기관 정보를 수집합니다.
Veeva Clinical Operations 소개
Veeva Clinical Operations는 단일 통합 플랫폼을 통해 임상팀의 효율적인 임상시험 실행을 지원합니다. 스터디 스타트업 부터 종료까지 프로세스를 간소화하고 데이터 가시성을 개선하면 스폰서, 기관, CRO 전반의 일정이 가속화되고 협업이 향상됩니다.
