Veeva Clinical Data
最新の臨床試験のための
クリニカルデータ
患者、治験実施医療機関、スポンサー間で
シームレスに接続されたデータフロー
Veeva Clinical Data
今日のクリニカルデータのジャーニーは、新たな複雑さと労力をもたらしています。患者、治験実施医療機関、スポンサーはより多くのデータに囲まれており、テクノロジーはしばしば負担を増やすだけです。Veeva Clinical Data アプリケーションは、すべてのユーザーのデータ収集と処理を簡素化します。
患者の臨床試験参加を容易に
Veeva eCOA を使用すると、患者はどのデバイスでも動作する単一のアプリで、今後予定されているすべての調査にアクセスし、完了することができます。患者は、試験期間中、同意書を記入し、試験文書にアクセスすることができます。
治験実施医療機関の労力を軽減
Veeva EDC は、ユーザーが保留中のアクションやダイナミックケースブックなど、重要なことに集中できるようにします。Veeva はまた、治験実施医療機関にシングルサインオン体験を提供する VeevaID のような無料ソフトウェアも提供しています。
スポンサーのスピードと効率の向上
Veeva CDB を使用すると、データマネージャーはすべてのスタディデータを1か所に集約し、クリーニングします。プラットフォーム接続により、Veeva EDC と CTMS や Safety などのシステム間で重要なデータが自動的に転送されます。
Veeva EDC
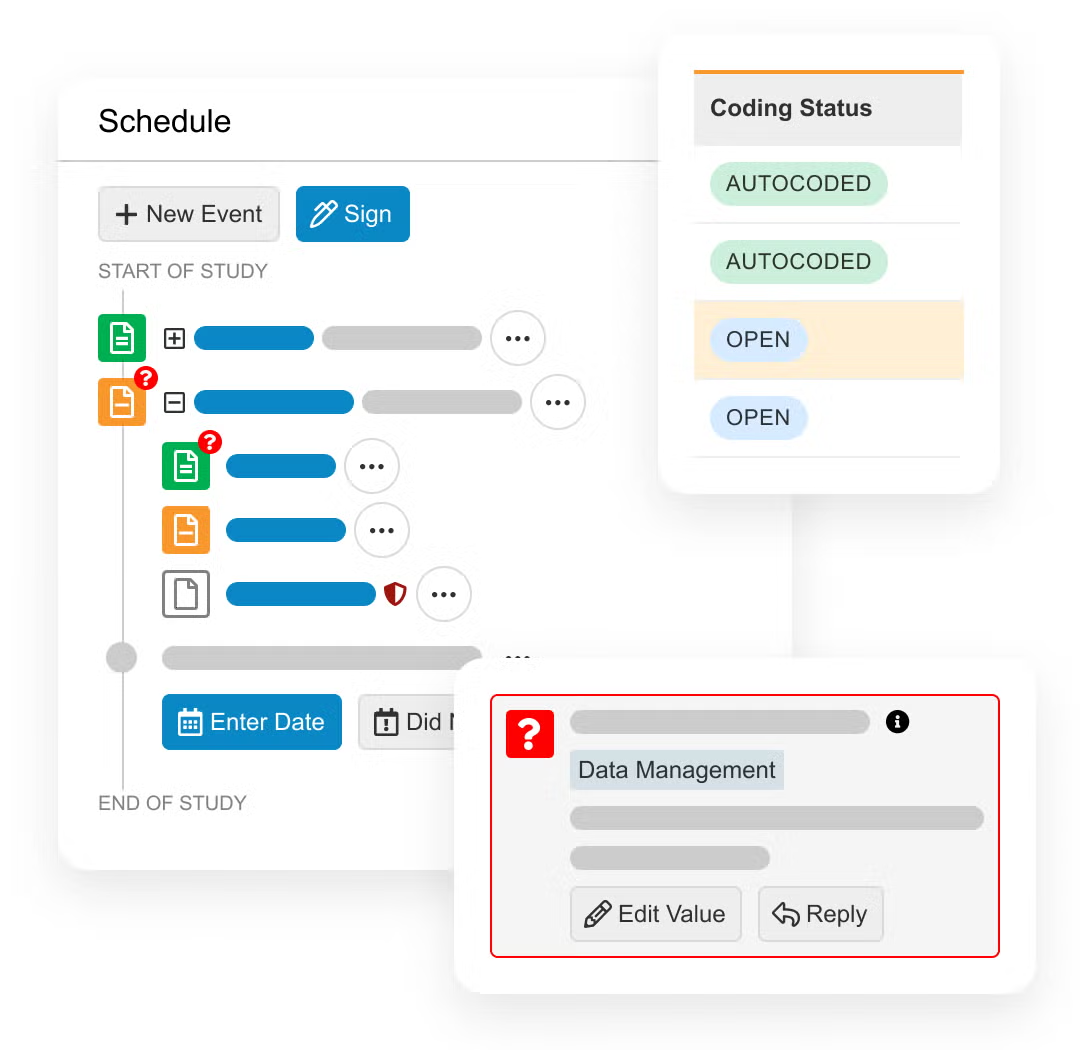
クリニカルデータマネジメントのサイクルタイムと労力を 50% 以上削減します。従来の EDC とは異なり、Veeva EDC はシステム内の仕様、ライブデザインレビュー、ターゲット UAT により、より迅速なスタディ構築を可能にします。Veeva EDC では、カスタムファンクションは不要で、プロトコル改訂が生じた場合でも、ダウンタイムを発生しません。
詳細はこちらVeeva CDB
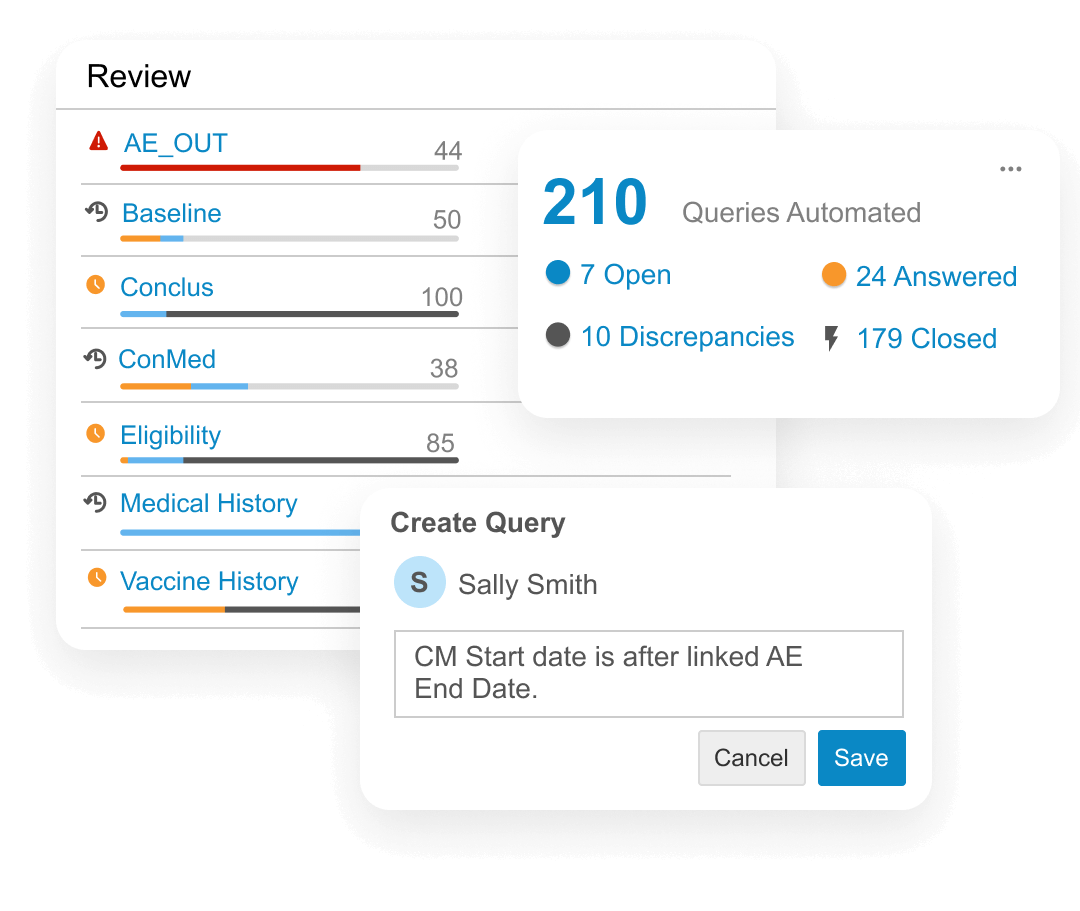
Veeva のクリニカルデータワークベンチを使用して、完全かつ同時にデータアクセスできます。EDC とサードパーティのデータは 1 か所に集約され、自動化によりデータクリーニングの労力が最大50%削減されます。
詳細はこちらVeeva eCOA
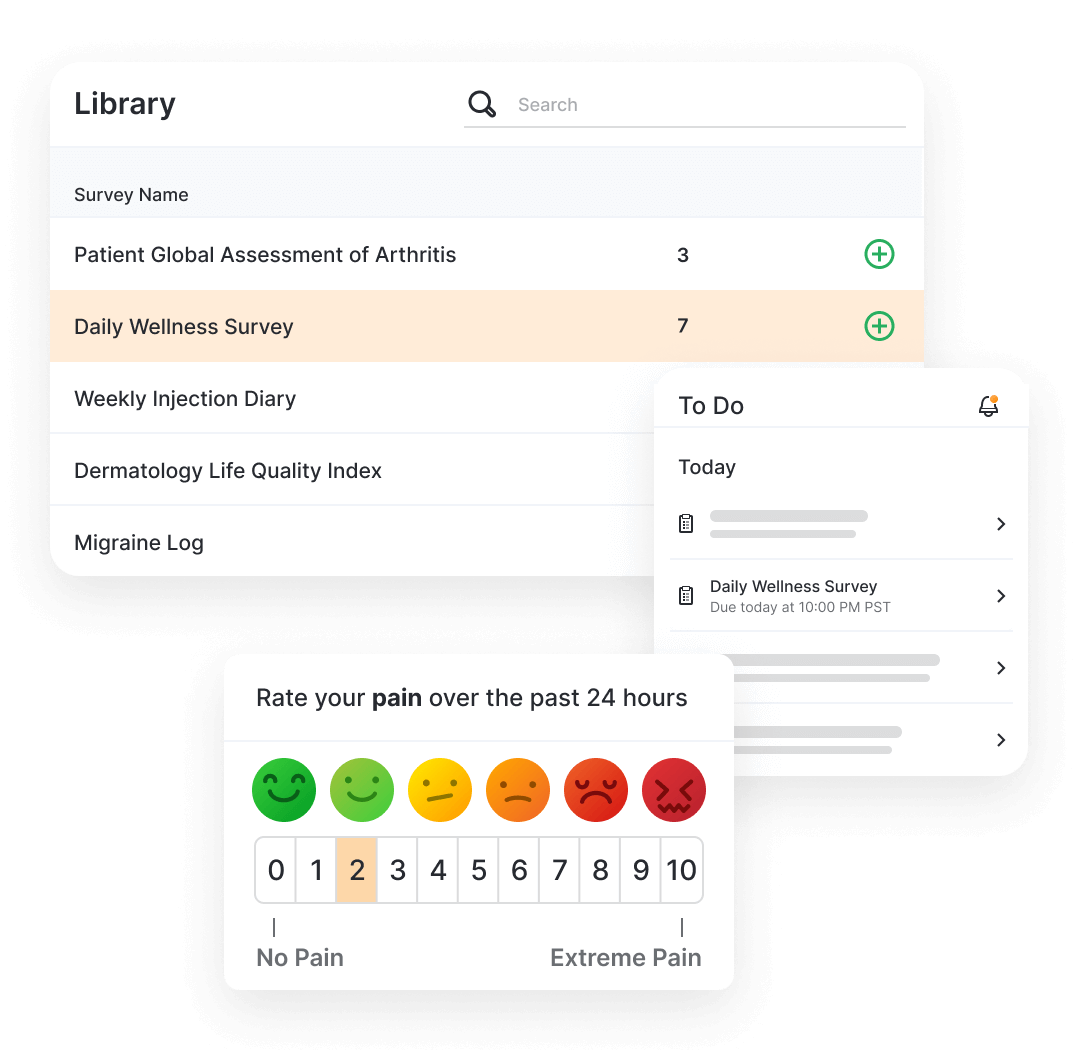
単一のアプリで臨床試験参加者から直接アンケートの回答を収集します。現代的なデザイナと、完全に再利用可能な ePRO および eClinRO のライブラリにより、試験を迅速に構築・管理できます。
詳細はこちらVeeva eConsent
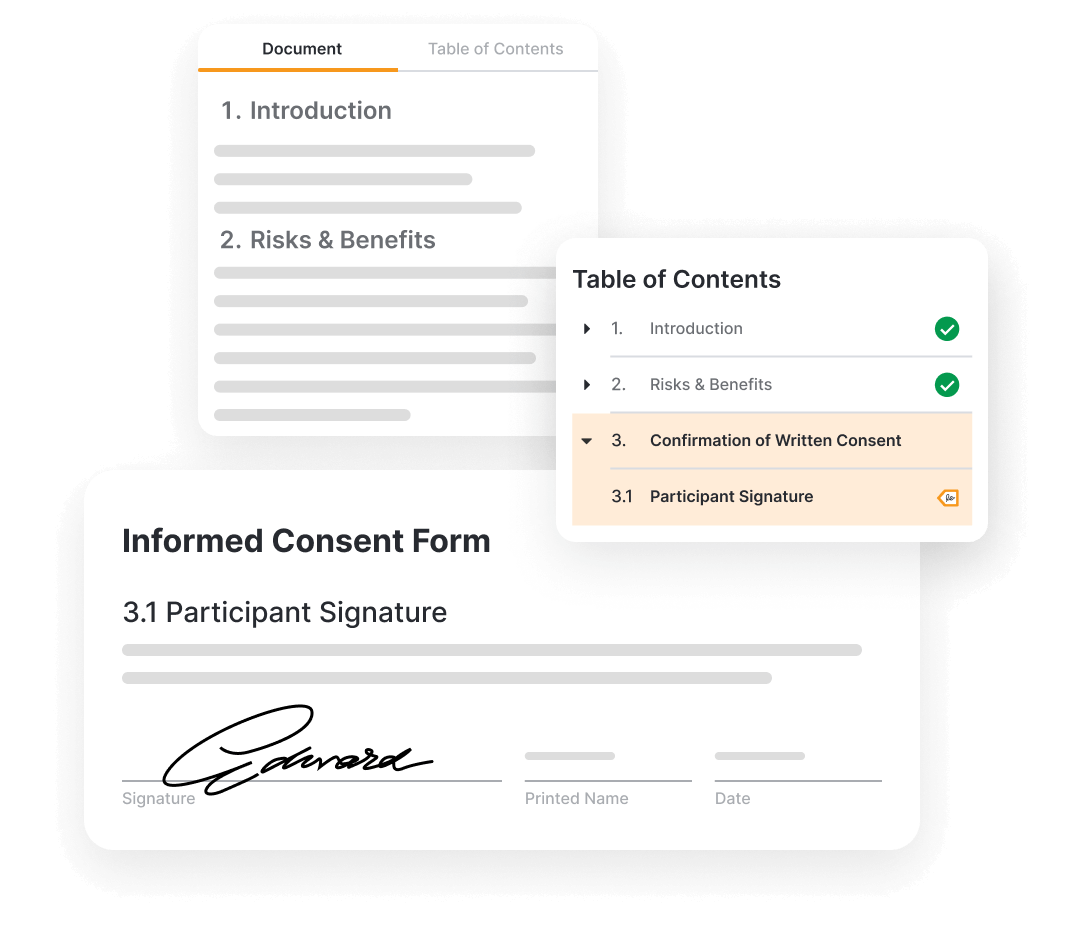
エンドツーエンドのプロセスにより、インフォームド・コンセントの設定、完了、レビューを簡素化し、管理負担を軽減し、治験実施医療機関と患者にとってより良い体験を提供します。
詳細はこちらVeeva Connections

Veeva Connections は Veeva が提供する統合機能で、Vault 間でデータやドキュメントをシームレスに転送します。クリニカルデータマネジメントチームにとって、Clinical Ops-EDC Connection は最新の施設情報を提供します。Veeva RTSM-EDC Connection は、治験実施医療機関による重複したデータ入力の必要性を排除し、データマネジメントチームによる関連する照合作業を軽減します。Veeva CDB-eCOA Connection は、患者入力データを転送して他のデータソースと照合し、傾向を特定します。その他の Veeva Connections については Veeva Development Cloud をご覧ください。
従来のプロセスを再定義するイノベーション
Veeva Clinical Data は、今日の臨床試験のペースを加速し、複雑さを軽減します
構築時間を短縮
スタディ途中の変更にかかる労力を削減
データクリーニングサイクルタイムを短縮
Customer Validation
Innovative companies are seeing the difference.










リソース




