Veeva QualityDocs
安全で効率的な GxP コンテンツ管理
QualityDocs は規制対象の品質コンテンツの管理ソリューションです。Veeva 独自の GxP コンテンツ参照モデルをベースに、ベストプラクティスと標準化を実現します。本アプリケーションは、コンテンツの作成から廃棄までのライフサイクル全体わたって管理します。社内外の関係者がシステム内の管理された環境下で直接連携し、品質契約書やバッチ関連文書などの情報を共有することができます。
Announced 2013 Status Very Mature Customers 100+
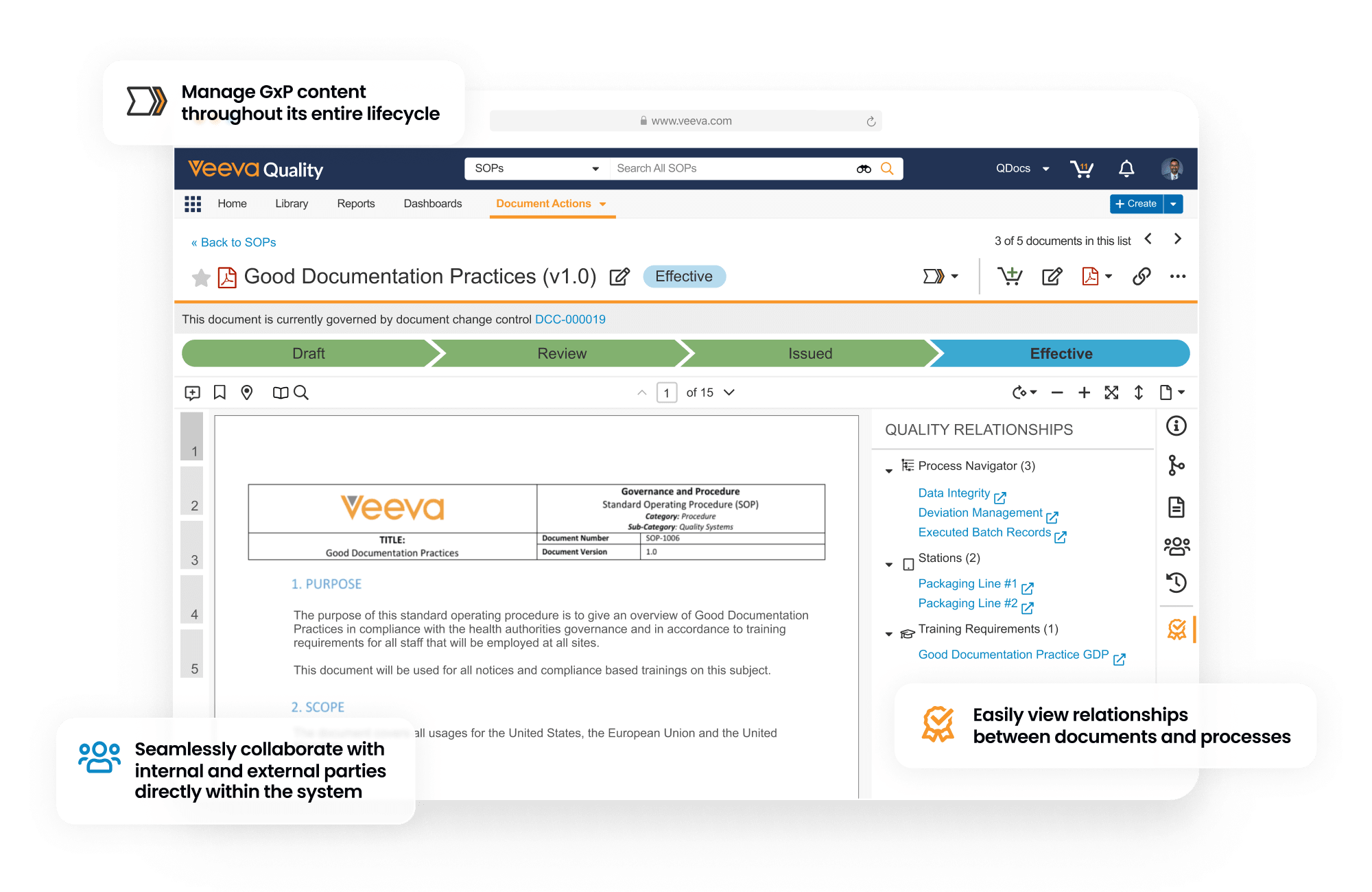
安全な情報共有と連携により、品質業務を効率化
Veeva AI for Quality
デモを見る
ドキュメント翻訳エージェント
SOPなどのドキュメントを多言語に翻訳することで、業務サイクル全体を効率化し、所要時間の短縮を実現。
Why Veeva QualityDocs
査察対応を 50% 高速化
Customer Success
500 社を超える企業が、
Veeva QualityDocs で GxP コンテンツを管理