記事
レガシーツールからの脱却:バイオ医薬品企業および CRO 5 社における最新 EDC の活用事例
従来の電子データ収集(EDC)システムには、今日の臨床試験で要求される複雑なプロトコルや頻繁な修正に対応するには柔軟性が欠けています。そうしたレガシーツールは、隠れたデータ管理問題を生み出すことで臨床試験チームの業務を妨げ、臨床能力に影響を与えます。レガシーシステムを使用するデータマネージャーは、手作業による迂回措置(ワークアラウンド)を講じたり、カスタムプログラミングを行ったりする必要があり、それによってボトルネックが生じます。これは、熟練したリソースの圧迫、臨床知見の遅れ、スタディコストの増加につながります。
データ管理業務を社内で移行するにせよ、医薬品開発業務受託機関(CRO)パートナーに別システムへの移行を依頼するにせよ、スポンサーは臨床データをより管理しやすくする方法を模索しています。多くのユーザーがレガシーベンダーによる移行またはアップグレードの必要に迫られる中、最新のアジャイルEDCシステムに切り替える時期が来ています。
臨床試験環境全体にわたる標準化
データの所有権を再取得する方法は数多くありますが、共通する成功要因はデータマネジメントモデルの標準化です。
スイスに本社を置く中堅バイオ医薬品企業であるIdorsia Pharmaceuticals社は、以前はすべての臨床試験を外部委託していました。チームは臨床試験仕様書をCROパートナーに送り、仕様書を受け取ったCROパートナーはシステムでのスタディの構築、ユーザー受け入れテスト(UAT)の完了、SOPの遵守に責任を負い、臨床試験データをIdorsia社に戻します。しかし、4社のCROパートナーを相手に5種類のEDCシステムを使用することで、監視が困難なレベルまでデータマネジメントモデルが分断化されていることが次第にわかってきました。データマネジメントおよびプログラミング担当ディレクターのVincent Rolland氏は、当時のことを次のように振り返っています。「当社の標準eCRF(電子症例報告書)は、CROやEDCシステムごとに調整する必要がありました。そのため、かなりの頻度で『車輪の再発明』を強いられていました。」
「この新しいモデルにより、標準化とデータ管理のメリットが余すところなく得られ、社内SOPを使って当社プロセスについてCROパートナーをトレーニングできます。」
Idorsia Pharmaceuticals社、データマネジメントおよびプログラミング担当ディレクター
Vincent Rolland氏
そこで、Idorsia社はEDC構築の内製化を選択し、スタディデザインをVeeva Vault CDMSで直接行えるようにすることにしました。すべてのスタディで同じツールを使用することで効率が高まり、UATプロセスの迅速化、ドキュメント生成時の自動化の拡大、エディットチェックの削減を通じて時間が節約されました。「この新しいモデルにより、標準化とデータ管理のメリットが余すところなく得られ、社内SOPを使って当社プロセスについてCROパートナーをトレーニングできます」とRolland氏は付け加えます。
Idorsia社とは異なる道筋をたどって、標準化を通じてデータ管理を強化したスポンサーもあります。ある中堅バイオ医薬品企業(本社:ヨーロッパ)は、データマネジメントの多くの側面を含め、臨床試験の大部分を外部委託しています。同社は、Vault EDCを導入すると同時に、構築の内製化、一部外部委託、および完全外部委託のスタディ環境に柔軟に対応できるeCRF標準を構築しました。特にCROを使用する場合、グローバルライブラリーを早期に構築すると時間を節約できることがわかりました。
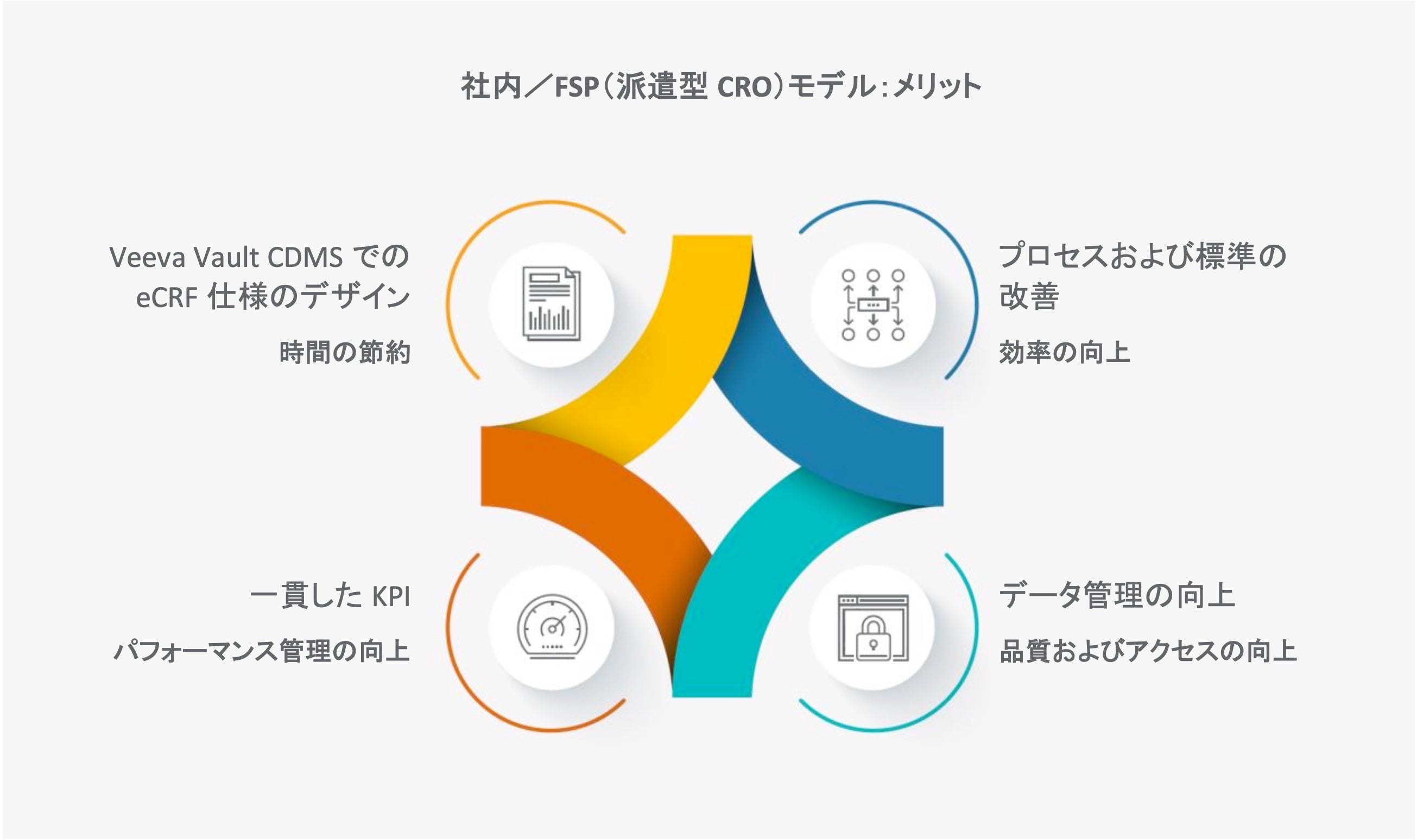
スポンサーとCROにとっての継続的なメリット
データマネジメント活動の大部分を外部委託するスポンサーは、パートナーのテクノロジー選択の最終受益者(または犠牲者)です。CROが手作業主体のレガシーシステムに頼っている場合、結果として上市の遅れやコストの増加を招きます。逆に、CROに使用させたいEDCシステムをスポンサーが規定する場合、双方にメリットがあります。
「場合によっては、EDCデータベースの構築時間を最大50%短縮することができました…さらに、スポンサー側でも30%のコスト削減が認められています。」
Syneos Health社、臨床データマネジメント担当シニアディレクター
Trevor Griffiths氏
CROのSyneos Health社は、テクノロジーをバイオ医薬品企業のために実施する臨床試験の重要な加速要因と見ています。同社は、最新のEDCシステムがデータマネージャーの日常業務にもたらす変化を直接経験しています。カスタムファンクションから移行する(そしてその代わりにVault EDC内で動的ルールとチェックを設定する)ことで、スタディ構築期間を大幅に短縮しました。同社臨床データマネジメント担当シニアディレクターのTrevor Griffiths氏は、次のようにコメントしています。「場合によっては、EDCデータベースの構築時間を最大50%短縮することができました…さらに、スポンサー側でも30%のコスト削減が認められています。」
「そうした効率向上を実現できたのは、システム設計によって品質に集中できるようになったからです。」
Fortrea社、データマネジメント担当ヴァイスプレジデント
Jerry Yarem氏
グローバルCROのFortrea社も同様に、顧客サービスと競争力の向上を望んでいました。そこで、EDCとRTSMから臨床試験管理システム(CTMS)と電子治験マスターファイル(eTMF)に、臨床インフラを統合することにしました。最新のEDCを採用することで、同社はプログラミングと手作業にかかる時間を最小限に抑えると同時に、独自フォームの使用を20〜30%削減することができました。Fortrea社のデータマネジメント担当ヴァイスプレジデントのJerry Yarem氏は、次のようにコメントしています。「そうした効率向上を実現できたのは、システム設計のおかげで品質に集中できるようになったからです。」
CROのBioforum社もまた、先進的で使いやすい構築ツールを備えたEDCにアップグレードすることで、顧客のスケジュール短縮とコスト削減を実現しました。同社のチーフデータストラテジスト兼ソリューションオフィサーのTanya du Plessis氏は次のようにコメントしています。「Vault EDCはよりアジャイルであり、大幅な迅速化を実現する環境を提供してくれます。スタディデザインが複雑だからといって、複雑な構築が必要だとは限りません。従来のカスタムファンクションでは、構築だけでなく検証や修正のために多くの遅延が発生します。カスタムファンクションを排除し、ルールを使用することはゲームチェンジャーとなります。複雑なスタディデザインでも構築が容易です。」
最新のシステムアーキテクチャは、CROと顧客のコラボレーションを支援します。同氏は次のようにコメントしています。「スポンサーがPDFやプリントアウトではなく、システムで直接レビューできることは非常に効果的です。スポンサーが変更を希望する場合、その仕組みを即座に示すことができます。そのためコミュニケーションが容易になり、最初から正しく理解するのに役立っています。」
「Vault EDCのスピードと柔軟性は、スケジュールの短縮に非常に有利です。Veevaを使用すると、修正が他のプラットフォームに比べて70%迅速化されます。」
Bioforum社、チーフデータストラテジスト兼ソリューションオフィサー
Tanya du Plessis氏
これらのメリットは、立ち上げ時だけでなくスタディ期間中もずっと続きます。同氏は次のようにコメントしています。「Vault EDCのスピードと柔軟性は、タイムラインを達成する上で非常に有利です。Veevaを使用すると、修正が他のプラットフォームに比べて70%迅速化されます。」
レガシーツールの限界
レガシーテクノロジーから脱却し、最新の標準化されたシステムを導入することには大きなメリットがあり、スポンサーとCROはさまざまなスタディ環境でそのメリットを享受しています。CRFが標準とプロトコルから直接構築されるため、かつては数カ月要していたスタディ構築が一貫して迅速かつ効率的になります。移行やダウンタイムを伴わない修正は、現代のスタディにおける長年の問題点に対処しています。
「実際、初めてでもとても楽しく容易にフォームやルールをデザインできます。ルールがフォームデザインに組み込まれているため、エディットチェックを大幅に削減できます。しかも移行作業不要です。これはありがたいの一言に尽きます。」
中堅スポンサーのプリンシパルデータマネージャー
欧州の中堅スポンサーのプリンシパルデータマネージャーは、次のようにコメントしています。「実際、初めてでもとても楽しく容易にフォームやルールをデザインできます。ルールがフォームデザインに組み込まれているため、エディットチェックを大幅に削減できます。しかも移行作業不要です。これはありがたいの一言に尽きます。」
バイオ医薬品企業が Vault EDCに切り替えてスタディの迅速化と効率化を実現した理由 をお確かめください。
