Veeva Disclosures
臨床試験情報開示の一元化と合理化
プロセスを自動化し、正確で期限内の提出を確実にします
Announced 2023
Status Early
Customers 1-10
Veeva Disclosuresで複雑さを軽減し、申請を迅速化
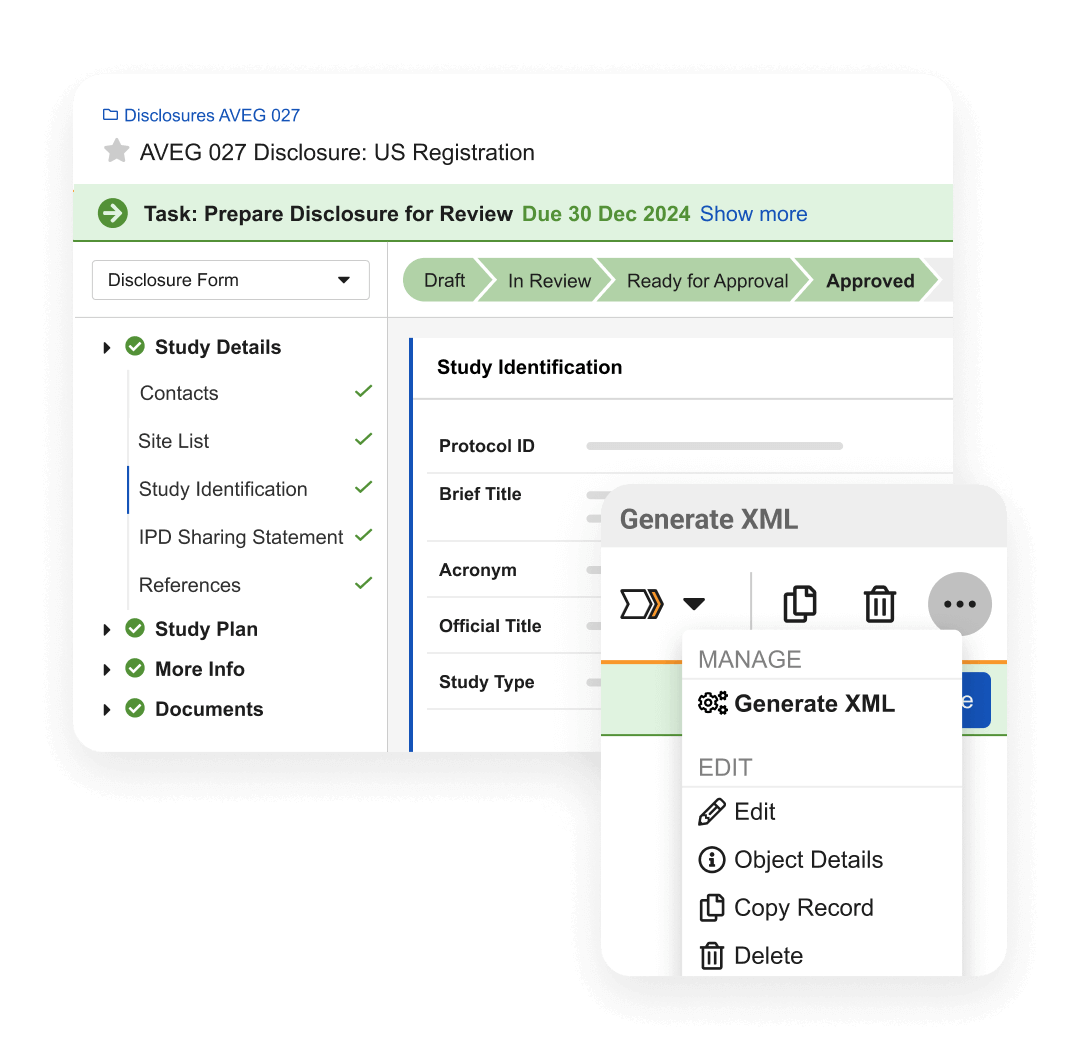
開示プロセスの管理
Veeva Disclosures は、レジストリとの試験登録および結果の開示の共有を管理します。取得、レビュー、ワークフロー、承認、報告、XMLの生成と提出など、プロセス全体をサポートします。
ルールとワークフローによる自動化
事前に設定されたレジストリルールにより、ユーザーは規制要件に簡単に準拠できます。試験データやマイルストーンの変更に対する自動アラートにより、ユーザーは重要なタスクについて通知を受け、行動を起こすことができます。Veeva eTMF での開示文書の自動ファイリングにより、提出証明を作成できます。
リアルタイムの可視化
レポートとダッシュボードにより、グローバルな申請状況、業務の進捗状況、主要なメトリクスを可視化します。
統一されたシステムの活用
Veeva Disclosures は Veeva eTMF、Veeva CTMS、Veeva Study Startup のデータを使用するため、サードパーティとの統合や手作業によるデータ入力が不要です。
Veeva Disclosuresが選ばれる理由
グローバルな情報開示を
一元管理
申請の迅速化
事前設定されたルール、国別情報、レジストリ更新の自動アラートにより、申請を迅速化します。コンプライアンスと監視の簡素化
データの検証、組み込みのバージョン管理、監査証跡により、正確性と透明性を向上させます。効率性と敏捷性の向上
リアルタイムの申請文書作成、ポイントアンドクリック構成、承認ワークフローにより、生産性を向上します。クリニカルオペレーションの統一
データと文書の再利用により、サードパーティとの統合を排除します。
